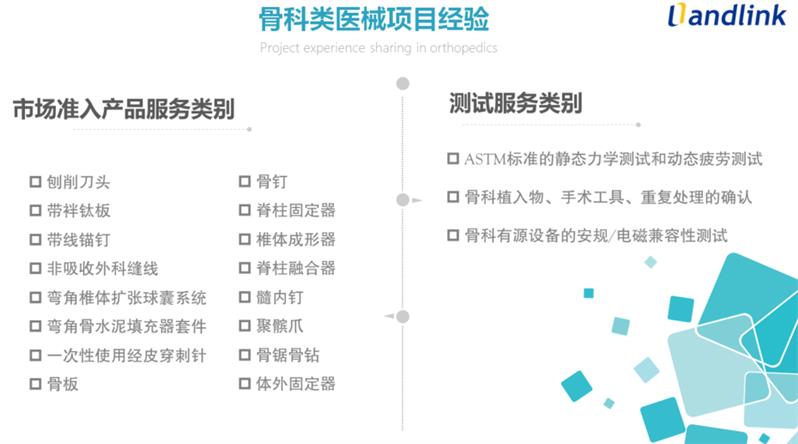
- 产品描述
欧盟器械法规外包服务
峦灵可以帮助您管理整个CE标志的全过程,包括:
—确定产品信息,选择适用的指令;
—器械的分类;
—帮助制造商建立质量管理体系,并评估运转的效果;
—准备注册文件,包括:技术文件和/或设计文档;
—提供欧盟授权代表的服务;
—帮助制造商选择合适的公告机构,并协助前期的沟通;
—协助制造商进行审核准备,指导制造商完成整改,已获取CE和ISO 13485证书;
— 帮助制造商起草符合性声明;
—评价CE标志的使用的规范性,避免因标志使用不规范导致的的投诉和召回。需要时,可提供欧盟成员国的产品注册或备案服务。
—产品上市后可以提供后续的法规较新服务。
合格评定程序-MDR
附录IX QMS+技术文件
- Chapter I: 质量管理体系
- Chapter II: 技术文件评审
- Chapter III: 行政规定
附录X 型式检查
附录XI 产品符合性验证
- Part A: 生产质量保证体系
- Part B: 产品验证
*) 针对MDR的I类灭菌、测量或重复使用产品,公告机构仅关注和保持无菌条件、计量要求和重复使用有关的内容。
-----------------------------------------
附录II 技术文件
附录III 有关上市后监督的技术文件
评价 - 总结
非用途器械有要求,应同时考虑CS的要求
GSPR 23.2 标签要求– ER 13.3
主要变化点
? 23.2 (d) 欧盟代表信息:MDD要求在标签、装或IFU中提供;MDR要求标签上必须提供,IFU未要求提供。
? 23.2 (e) 器械包含或采用药物、人源或动物源物质的信息。
? 23.2 (f) 根据GSPR 10.4.1提供器械包含CMR和干扰物的信息。
? 23.2 (h) UDI
? 23.2 (i) 器械安全使用或植入的时间限制,至少表示为与之相关的年份和月份
合格评定程序-MDD
I类 (S) I类灭菌器械
I类 (M) I类带测量功能的器械
附录II 全面质量保证体系,不包含II.4
附录II.4 EC 设计检查 (“设计文档评审”)
附录III EC 型式试验
附录IV EC 产品批检
附录IV (M) 测量功能部分的EC 产品批检
附录V 生产质量保证体系
附录V (S) 灭菌部分的生产质量保证体系
附录V (M) 测量功能部分的生产质量保证体系
附录VI 产品质量保证体系
附录VI (M) 测量功能部分的产品质量保证体系
附录 VII EC符合性声明
*) *公告机构进行评审.
**)对灭菌或测量方面的要求(见附录VII(5))
我们的团队大部分来自****的公告机构;
曾服务于**的器械企业●GE, AGFA, 微创,拥有平均15年以上器械法规经验;
从研发到上市,再到后市场服务,峦灵的专业团队为您提供**法规支持;
峦灵是行业内的咨询公司,汇聚了来自法规、等各领域对法规有深刻理解的人士及*,致力为企业提供一站式、*、系统化的技术咨询服务, 帮助企业向**市场提供安全、有效和合规的产品, 迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的产品迅速推向**市场。 我们的服务包括: 法规合规服务(CE认证、NMPA注册、FDA注册、**注册) 质量管理体系(ISO13485、NMPA GMP、MDSAP、FDA QSR820、质量体系日常维护服务); 测试服务(有源产品测试认证咨询、无源产品测试认证咨询、清洗消毒灭菌验证确认、定制化摸底测试服务) **注册(加拿大、澳大利亚、日本、巴西、韩国、俄罗斯、东南亚注等); 法规培训服务(企业定制培训、小班课培训)
欢迎来到上海峦灵医疗信息技术有限公司网站,我公司位于历史文化悠久,近代城市文化底蕴深厚,历史古迹众多,有“东方巴黎”美称的上海市。 具体地址是上海青浦公司街道地址,负责人是阮贞。
主要经营CE认证 FDA510K。
你有什么需要?我们都可以帮你一一解决!我们公司主要的特色服务是:CE认证,FDA注册,**注册等,“诚信”是我们立足之本,“创新”是我们生存之源,“便捷”是我们努力的方向,用户的满意是我们最大的收益、用户的信赖是我们最大的成果。
本页链接:http://www.cg160.cn/vgy-54879126.html
以上信息由企业自行发布,该企业负责信息内容的完整性、真实性、准确性和合法性。阿德采购网对此不承担任何责任。 马上查看收录情况: 百度 360搜索 搜狗
关于上海峦灵医疗信息技术有限公司
商铺首页 |
更多产品 |
联系方式
峦灵是行业内的咨询公司,汇聚了来自法规、等各领域对法规有深刻理解的人士及*,致力为企业提供一站式、*、系统化的技术咨询服务, 帮助企业向**市场提供安全、有效和合规的产品, 迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的产品迅速推向**市场。 我们的服务包括: 法规合规服务(CE认证、NMPA注..
- 我要给“锡林郭勒盟MDD法规”留言
- 更多产品
相关分类