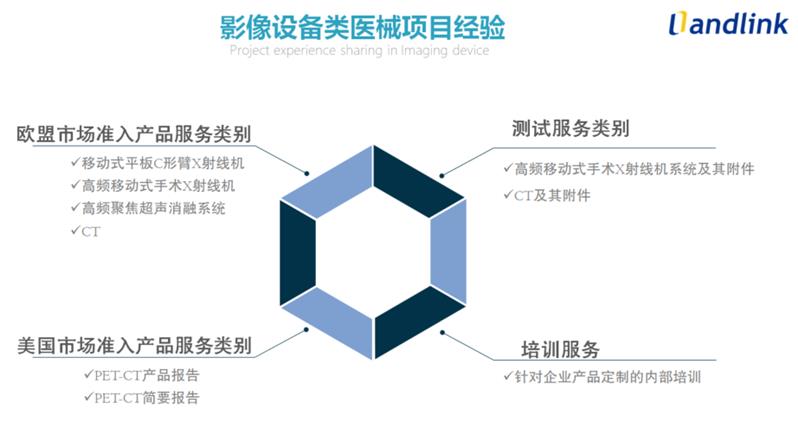
- 产品描述
欧盟器械法规外包服务
峦灵可以帮助您管理整个CE标志的全过程,包括:
—确定产品信息,选择适用的指令;
—器械的分类;
—帮助制造商建立质量管理体系,并评估运转的效果;
—准备注册文件,包括:技术文件和/或设计文档;
—提供欧盟授权代表的服务;
—帮助制造商选择合适的公告机构,并协助前期的沟通;
—协助制造商进行审核准备,指导制造商完成整改,已获取CE和ISO 13485证书;
— 帮助制造商起草符合性声明;
—评价CE标志的使用的规范性,避免因标志使用不规范导致的的投诉和召回。需要时,可提供欧盟成员国的产品注册或备案服务。
—产品上市后可以提供后续的法规较新服务。
GSPR 23.3 无菌包装的标签要求
主要变化点:? 23.3 (a) 允许无菌包装识别的标识
? 23.3 (b)声明该器械处于无菌状态
? 23.3 (c) 灭菌方法
? 23.3 (d) 制造商的名称、
? 23.3 (e) 器械的描述
? 23.3 (f) 用于试验的器械,文字“仅用于试验”
安全和性能总结(SSCP)
? 制造商的职责:
- 负责起草SSCP
- SSCP的草稿应是CE技术文件的一部分,根据符合性评估程序提交给公告机构进行确认
- 制造商应在标签或说明书中告知可以获得SSCP的地方
- 至少每年较新一次
GSPR 21 供应能量或物质的器械的风险– ER 12.8,12.9
设计和制造:
21.1 应确保器械能够准确地设置和维持输送量,从而足以保证患者和使用者的安全。
GSPR 23.3 无菌包装的标签要求
? 23.3 (g) 顾客定制器械,文字“顾客定制器械”
? 23.3 (h) 制造日期的年和月
? 23.3 (i) 清晰地指明使用或安全植入器械的时间期限,至少包括年、月。
? 23.3 (j) 提示使用者应检查使用说明书,以了解若无菌包装损或在使用前不小心打开,该如何处理。
? Note: 相比MDD,把无菌包装的要求单独罗列出来,大部分要求和MDD相似。
峦灵可以帮助您管理整个CE标志的全过程,包括:
—确定产品信息,选择适用的指令;
—器械的分类;
—帮助制造商建立质量管理体系,并评估运转的效果;
—准备注册文件,包括:技术文件和/或设计文档;
—提供欧盟授权代表的服务;
—帮助制造商选择合适的公告机构,并协助前期的沟通;
—协助制造商进行审核准备,指导制造商完成整改,已获取CE和ISO 13485证书;
— 帮助制造商起草符合性声明;
—评价CE标志的使用的规范性,避免因标志使用不规范导致的的投诉和召回。需要时,可提供欧盟成员国的产品注册或备案服务。
—产品上市后可以提供后续的法规较新服务。
峦灵是行业内的咨询公司,汇聚了来自法规、等各领域对法规有深刻理解的人士及*,致力为企业提供一站式、*、系统化的技术咨询服务, 帮助企业向**市场提供安全、有效和合规的产品, 迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的产品迅速推向**市场。 我们的服务包括: 法规合规服务(CE认证、NMPA注册、FDA注册、**注册) 质量管理体系(ISO13485、NMPA GMP、MDSAP、FDA QSR820、质量体系日常维护服务); 测试服务(有源产品测试认证咨询、无源产品测试认证咨询、清洗消毒灭菌验证确认、定制化摸底测试服务) **注册(加拿大、澳大利亚、日本、巴西、韩国、俄罗斯、东南亚注等); 法规培训服务(企业定制培训、小班课培训)
欢迎来到上海峦灵医疗信息技术有限公司网站,我公司位于历史文化悠久,近代城市文化底蕴深厚,历史古迹众多,有“东方巴黎”美称的上海市。 具体地址是上海青浦公司街道地址,负责人是阮贞。
主要经营CE认证 FDA510K。
你有什么需要?我们都可以帮你一一解决!我们公司主要的特色服务是:CE认证,FDA注册,**注册等,“诚信”是我们立足之本,“创新”是我们生存之源,“便捷”是我们努力的方向,用户的满意是我们最大的收益、用户的信赖是我们最大的成果。
本页链接:http://www.cg160.cn/vgy-54537827.html
以上信息由企业自行发布,该企业负责信息内容的完整性、真实性、准确性和合法性。阿德采购网对此不承担任何责任。 马上查看收录情况: 百度 360搜索 搜狗
关于上海峦灵医疗信息技术有限公司
商铺首页 |
更多产品 |
联系方式
峦灵是行业内的咨询公司,汇聚了来自法规、等各领域对法规有深刻理解的人士及*,致力为企业提供一站式、*、系统化的技术咨询服务, 帮助企业向**市场提供安全、有效和合规的产品, 迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的产品迅速推向**市场。 我们的服务包括: 法规合规服务(CE认证、NMPA注..
- 我要给“神农架CE技术文件”留言
- 更多产品
相关分类