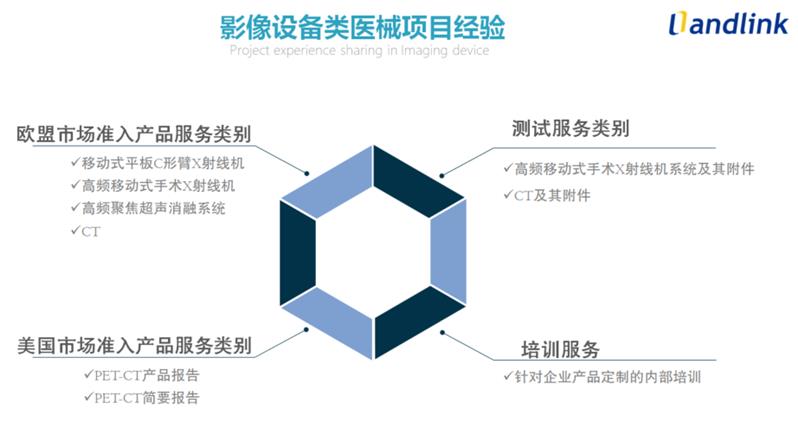
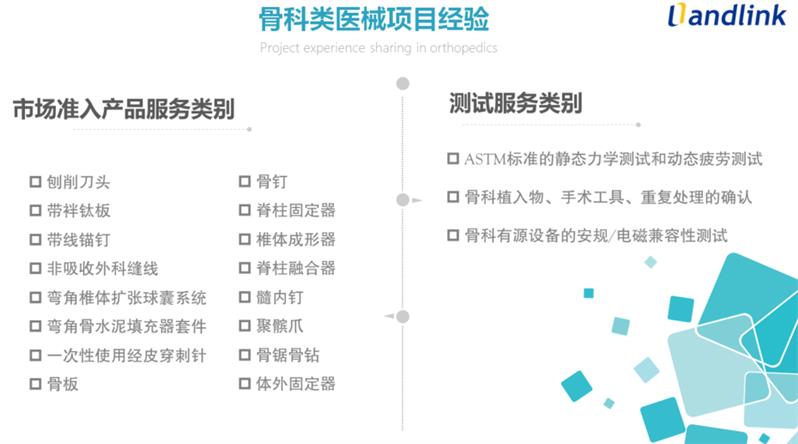
- 产品描述
MDR法规学习目的:
了解MDR相比MDD的主要变化。
具体了解MDR下获取CE标志的主要过程及其变化,特别是上市前活动、技术文件、评价、上市后监督、警戒系统。
能够识别MDR对质量管理体系的影响并制定应对措施。
能够规划MDR过渡期的安排。
GSPR 17 电子可编程系统和软件– ER
17.1 电离辐射
• 设计应当保证重复性、可靠性和性能。
• 当发生单一故障时,应当采取适当的措施,尽可能地消除和减少风险
23.4 (s) (续)相关情况下,允许使用者向患者简述警告、注意事项、禁忌
症、待采取措施以及与器械有关的使用限制,酌情包括:
• 器械故障或可能影响安全的性能变化;
• 暴露在合理可预见的外部影响和环境条件,例如:…与诊断和有关的辐射…
• 器械对其他设备的干扰,如电磁干扰;
• 给药器械在选择输送物质时的任何限制或不相容性;
• 与作为器械组成部分的药物或生物材料的警告、注意事项和/或限制
• 含CMR、干扰物或可能引起病人或使用者的致敏/反应的注意事项。
MDR适用的产品范围扩大
• 采用非活性的人类来源的组织或物制造的器械(Art. 1)
• 疾病的预测和预后(Art. 2)
• 用于直接的功能的产品 => 附件(Art. 2)
• 非用途的器械(Annex XVI)
GSPR 23.1 制造商提供的信息 – 通用要求
• 各器械应附有识别器械及其制造商所需的信息,并酌情将安全与性能信息传达给使用者或其他人。
• 此类信息可能出现在器械本身、包装上或使用说明书中,*若制造商有网站,则应在网站上提供并保持较新信息。
关于我们:峦灵是行业内的器械咨询公司,汇聚了来自器械法规、等各领域对法规有深刻理解的人士及,致力为器械企业提供一站式、、系统化的技术咨询服务。迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的器械产品迅速推向**市场。
峦灵是行业内的咨询公司,汇聚了来自法规、等各领域对法规有深刻理解的人士及*,致力为企业提供一站式、*、系统化的技术咨询服务, 帮助企业向**市场提供安全、有效和合规的产品, 迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的产品迅速推向**市场。 我们的服务包括: 法规合规服务(CE认证、NMPA注册、FDA注册、**注册) 质量管理体系(ISO13485、NMPA GMP、MDSAP、FDA QSR820、质量体系日常维护服务); 测试服务(有源产品测试认证咨询、无源产品测试认证咨询、清洗消毒灭菌验证确认、定制化摸底测试服务) **注册(加拿大、澳大利亚、日本、巴西、韩国、俄罗斯、东南亚注等); 法规培训服务(企业定制培训、小班课培训)
欢迎来到上海峦灵医疗信息技术有限公司网站,我公司位于历史文化悠久,近代城市文化底蕴深厚,历史古迹众多,有“东方巴黎”美称的上海市。 具体地址是上海青浦公司街道地址,负责人是阮贞。
主要经营CE认证 FDA510K。
你有什么需要?我们都可以帮你一一解决!我们公司主要的特色服务是:CE认证,FDA注册,**注册等,“诚信”是我们立足之本,“创新”是我们生存之源,“便捷”是我们努力的方向,用户的满意是我们最大的收益、用户的信赖是我们最大的成果。
本页链接:http://www.cg160.cn/vgy-58429293.html
以上信息由企业自行发布,该企业负责信息内容的完整性、真实性、准确性和合法性。阿德采购网对此不承担任何责任。 马上查看收录情况: 百度 360搜索 搜狗
关于上海峦灵医疗信息技术有限公司
商铺首页 |
更多产品 |
联系方式
峦灵是行业内的咨询公司,汇聚了来自法规、等各领域对法规有深刻理解的人士及*,致力为企业提供一站式、*、系统化的技术咨询服务, 帮助企业向**市场提供安全、有效和合规的产品, 迄今为止,我们已与众多公司开展合作, 协助他们将安全、有效、合规的产品迅速推向**市场。 我们的服务包括: 法规合规服务(CE认证、NMPA注..
- 我要给“铜川MDR认证机构”留言
- 更多产品
相关分类