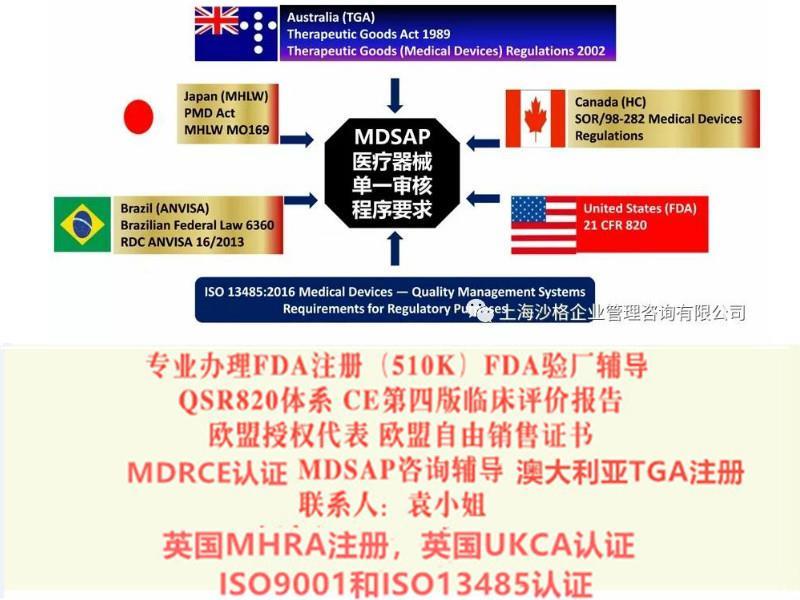
- 产品描述
我公司 FDA注册,FDA验厂、器械FDA QSR820验厂、OTC CGMP验厂及食品FDA验厂 、培训、翻译,FDA警告信处理,FDA黑名单移除
我公司有丰富的器械FDA QSR820验厂、OTC CGMP验厂及食品FDA验厂经验,师资源既具备深厚的法规背景知识,又具备非常强的专业英文能力,与FDA的沟通非常顺畅,对于FDA的审核思路和开具不符合的意思理解深刻,整改到位。
出口:美国FDA注册(含FDA510K申请)、 FDA QSR820验厂及整改、FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改、CE认证(CE整套技术文件编订、 CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016、欧盟授权代表、欧盟销售证书、英国BRC认证,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证(89/686/EC个人防护指令)。
QSR820验厂结果
1.没有任何书面评价,这是的情况;
2.轻微项的483表,或一封感谢信;
3.有批评的483表,它可能会导致:
1)Seizure(查封)
2)Detention(扣押)
3)Restraining Orders and Injunctions(强制停产)
4)Penalties(罚款)
5)Recall(撤回)
4. Waring letter(警告信)
QSR820验厂重点
审查重点
1.评审文件( or sampling)
2.QSIT方法(Quality System Inspection Technique)
4个主要子系统(nagement, Design, CAPA, P&PC)
3个辅助子系统(Documentation, terial, and Facility & Equipment Controls)
3.抱怨和投诉
4.仓库
5.测量设备
6.卫生的特殊要求,
7.特殊过程,包括软件
8.设计变更:工程变更,材料更改
9.过程确认
QSR820验厂经验
经验分享:
1、 企业生产及出口美国的量越大,用户抱怨越多,被FDA查厂的可能性越大;
2、 但(含港澳台)的企业,无论是一类,还是二类,三类,被FDA查厂的概率非常大, 本公司接触到大量低风险产品验厂的案例;
3、 所有检查费、、差旅、五星酒店、餐费等所有费用均由FDA承担;
4、 FDA通常提前1-3个月通知验厂,但不会通知具体到厂日期;
5、 通常FDA只来一个人,正常审核4天;
6、 质量手册、程序文件等重要文件需翻译成英文,环境卫生要搞好;
7、 FDA较强调内审及记录、相关部门的签字;
8、 FDA非常重视法律法规、专业知识、作业指导原则等员工培训与执行、签字;
9、 如有不符合项,审核员会现场开出483表;
10、 审核员提出的所有问题,企业必须在规定时间内提交书面回复,越快越好;
11、 重大不符合项,审核员会现场开出警告信(Warning letter),企业须在规定时间内完成整改;在此整改期间:
(1)对国外厂商,所有产品到达美国海关将自动扣留
(2)对美国厂商,FDA将通知其他部门,以供其在采购招标时考虑
(3)对美国厂商,FDA将暂停其出口许可证的审批
12、 如拒绝FDA验厂,或被发现与QSR 820严重不符项,工厂所有产品将被视为“假冒伪劣”
近几年,在美国以外的**市场,制造商的被抽样量一直稳居****。目前在FDA的注册制造商约为4500家左右,每年抽查的概率在2-3%。通常FDA工厂审查会由1名审查官进行为期4天的现场审查。制造商*支付任何审查费用。
FDA验厂步骤:
首先做好提前准备检查接待,建立一个检查应对管理小组,内部审计项目,模拟检查项目。
检查时间及,一般来说一类二类器械均为1名检察官;三类器械为1名或2名检察官,4-5个工作日。
评审文件:FDA检察官到现场,首先会评审文件,按QSIT方法--基于7个子系统4个主要子系统(管理、设计、纠正预防、生产过程);3个支持子系统(文件、物料、生产工具和设备控制);FDA检查工作时会以点带面,抓住一点,可在一个问题上几个来回,也可能检查整个公司的质量管理体系。
现场检查,注意检察官都特别警觉,能从周围环境中获取信息,融合信息进行判断。他们会阅读看到的文件包括公告,桌面上的文件等。有时候这些里面含有未被批准或者未被记载的章程,不受控的安全事宜,比如。确保员工有这种意识,随意流露出的信息不应该给检察官造成误导,文件不受控或者不安全,检察官在的地方不应该有多余文件。
检查结束前会有末次会议。末次会议有公司参加以表明公司对合规性的重视。末次会议期间检察官会提供FDA- 483 表格,里面有缺陷列表。检查483表格,如果有含糊的问题请跟检察官澄清,记录所有检察官对问题的答复。如果有明显的误解,请友好指出并提供证据。在器械检查中公司可以选择是否对483表格注解。
检查结果无非有:
没有483表格
483表格只含有微小缺陷,无不符合性历史和警告信
483表格有重大缺陷和警告性
438表格有重大缺陷,鉴于之前的不符合性和警告性会导致较严重的法律制裁
法律制裁有:禁令,扣押,罚金和进口滞留。
给483表格书面答复很重要,一般15天内答复。(虽然15天答复不是强制要求,是一般规律)。请确保完整全面答复,答复中应包含纠正措施的书面证据。
我们提供验厂服务包含:
a. 现已有质量管理体系与法规要求的差距
b. 过程的整体设计,包括现场的整改以及文件化体系以及应用的整改;
c. 基于FDA审核要求文件记录审阅、检查生产全过程GMP/QSR820等体系建立与维持,师与企业相关人员一起进行文件系统修整;
d. 帮助企业发现车间和仓库的不足与整改;
e. 对企业人员进行迎接审核技巧的培训;
f. 体系有效性的检查,在FDA来审核之前,安排本公司评审员进行模拟审核;
g. 陪同FDA验厂、担当翻译;
h. 协助企业进行不符合项的整改.
i. 确保顺利通过FDA验厂
注意事项
拒绝FDA验厂,后果很严重,可能会导致制造商丢掉原有的大片美国市场,造成很大的损失。
FDA审查官发现了工厂的管理系统有违背FDA的质量体系法规的内容,进而开具了书面形式的不符合项,也可以开具了“483”表。只要工厂按照FDA的要求积极整改,提供充分的证据,都不会导致更多后果。
我公司 FDA注册,FDA验厂、器械FDA QSR820验厂、OTC CGMP验厂及食品FDA验厂 、培训、翻译,FDA警告信处理,FDA黑名单移除
我公司有丰富的器械FDA QSR820验厂、OTC CGMP验厂及食品FDA验厂经验,师资源既具备深厚的法规背景知识,又具备非常强的专业英文能力,与FDA的沟通非常顺畅,对于FDA的审核思路和开具不符合的意思理解深刻,整改到位。
出口:美国FDA注册(含FDA510K申请)、 FDA QSR820验厂及整改、FDA警告信应对&RED LIST REMOVAL/QSR820体系/OTC验厂及整改、CE认证(CE整套技术文件编订、 CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016、欧盟授权代表、欧盟销售证书、英国BRC认证,BSCI验厂;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证(89/686/EC个人防护指令)。
FDA-QSR820验厂
美国的器械法规体系
美国食品品监督(FDA)是负责器械管理的机构。其根据各相关法律授权而制定的各类法规性的文件编为21CFRxxxx(xxxx为伯数字)。
QSR820
--又称21CFR820,是美国器械质量管理体系法规的英文缩写,因其位于美国联邦法规(Code of Federal Regulations)*21卷*820部分,故名;
--QSR820是美国(人用)器械制造商以及拟将产品销往美国的外国(人用)器械制造商必须遵守的质量管理体系法规,是多数器械在美国上市之前必须遵守、上市之后随时可能抽查的基本要求,这种抽查即通常所说的FDA器械QSR820验厂
--符合性检查:无论谁(FDA,或第三方机构)对工厂实施检查,都只是一个(针对相关法规的)符合性检查,不颁发任何证书,不属于认证活动。
谁应该遵守QSR820?
21QSR820.1规定:所有在美国和波多黎哥境内的,或有产品出口到美国和波多黎哥境内的器械企业,必须按QSR820的要求建立质量体系,企业可根据实际情况,满足QSR中与本企业制造活动相关的条款。
QSR820不适用
--不适用于器械零件生产商,但鼓励这类企业以QSR820中适用的条款为指导;
--不适用于人血和血制品生产商,这类企业应遵循21CFR606的规定。
谁负责验厂
FDA下属的CDRH(器械与放射健康中心)是专职负责器械企业管理的机构,其根据FDA的授权,安排检查员到各企业进行工厂检查。
验厂抽查原则
--根据法律规定,对未豁免QSR 820的产品的生产企业,进行例行检查;(大多数情况)
--II类器械或有510(K)注册的器械的企业,容易被抽到;
--为国外大公司做OEM的企业;
--产品在美国市场发生质量事故的企业。
检查频率及费用
美国境内企业:一般每两年检查一次;
美国境外企业:不定期检查;
所有检查费用由FDA承担。
第三方机构代为审查
在欧洲和美国本土(不适用于及港澳台企业),FDA也授权第三方机构进行工厂检查,委托企业需支付相应费用。这种委托第三方的检查只是个别的,仅适于FDA检查过并且无问题的企业,FDA对企业的工厂检查不委托任何第三方进行。
验厂指南
QSIT(质量体系检查技术)是FDA检查员的必修课程,也是FDA Quality Systems Inspection Reengineering Team专门编制的检查员手册,详细说明FDA审核员的检查方法、关注点。
SUNGO品牌创建于2006年,立志于成为化的法规技术服务商。我司可以办理:1:欧盟MDR CE咨询,MDR欧盟授权代表,欧盟注册2:欧盟IVDR CE咨询,IVDR欧盟授权代表,欧盟注册3:美国FDA注册,FDA510K4:国内的注册证和生产证5:加拿大的MDEL注册6:ISO13485咨询和认证目前SUNGO在中国、欧洲、北美和澳洲均设有服务机构,服务过的客户较是覆盖了(中国、越南、马来西亚、孟加拉、新加坡)、欧洲(英国、瑞士、瑞典、丹麦、挪威)、北美(美国、加拿大)、南美(阿根廷)、大洋洲(澳大利亚)和非洲(博茨瓦纳、南非)等国家和地区。SUNGO致力于为的生产商和经营者提供市场准入的合规咨询以及**注册服务。从产品生产、检测、过程管理、注册、认证、整改、上市跟踪等各环节为企业提供的技术支持,为产品合规和顺利上市保驾**。十多年里,SUNGO已为30多家上市公司和制造商,合计5000多家企业提供过相关服务。SUNGO始终追求支持、服务和客户满意。所有客户都有一对一的客服对接以保持经常性的联系,提供在线即时服务,针对贸易中存在的技术壁垒方面的问题提供的支持和解。选择SUNGO,不是选择了一次性的合作伙伴,而是选择了一个长期的技术支持的伙伴。我们将秉承一贯“服务、客户”的原则,依托的技术团队,优化我们的服务,让更多的器械合法、安全进入市场,为器械行业健康发展贡献力量。因为,所以放心!
欢迎来到上海沙格企业管理咨询有限公司网站,我公司位于历史文化悠久,近代城市文化底蕴深厚,历史古迹众多,有“东方巴黎”美称的上海市。 具体地址是黑龙江伊春金山屯公司街道地址,负责人是袁小姐。
主要经营上海沙格企业管理有限公司SUNGO是欧盟授权代表,从事FDA验厂、欧盟自由销售证书、医疗器械单一体系审核MDSAP、CE*四版临床评价报告、MDRCE认证、CE MDR认证、CE技术文件、EU 201。
我们公司主要提供商务服务 认证服务 等服务,我们确信,凭借我们的专业服务和良好的协调、沟通能力,定能使客户在经营生产中无后顾之忧,协助客户不断成长,在合作中与客户实现共赢。欢迎您致电咨询!
本页链接:http://www.cg160.cn/vgy-51147901.html
以上信息由企业自行发布,该企业负责信息内容的完整性、真实性、准确性和合法性。阿德采购网对此不承担任何责任。 马上查看收录情况: 百度 360搜索 搜狗
- 产品推荐
- 黔东南多群直播 多种方式录制 四川采光均匀度厂 室内照明检测 出具报告 江西多群同步 编辑课程 青岛市南区注册公司代理费用-来电咨询 高新区外贸公司注册从哪里机构申请 防爆CCC认证怎么办 攀枝花微信多群讲课 欢迎来电详谈 南城本镇区商标代理哪家服务好 来宾AI智能多群转发 朋友圈转发 海口软膏械字号产品批号申请价格 经验丰富 商洛熏蒸液消字号咨询 熟悉行业环境 熙悦汇代理财务外包服务
- 相关文章
- 胰岛素注射针清洗验证方案 UKCA证书 需要什么资料隔离衣的清洗验证方案 EC Rep 需要什么资料创可贴MHRA认证 MHRA注册 的关键纸尿裤MHRA认证 医疗器械产品MHRA注册 新规要求介绍颊面管MHRA注册 英国mhra注册 mhra如何申请电动救护车担架MHRA注册 MHRA认证注册 新规要求介绍手术衣的清洗验证方案 MDR CE证书 需要什么资料眼镜自由贸易证书 欧盟自由销售证书CFS 申请材料介绍病床自由销售证书 自由贸易证书 申请条件丁腈手套自由销售证书 CFS证书 有效期多久护具CFS证书 什么是欧盟自由销售证书 申请条件尿液分析仪美国FDA注册 什么是FDA注册流程
关于上海沙格企业管理咨询有限公司
商铺首页 |
更多产品 |
联系方式
SUNGO品牌创建于2006年,立志于成为化的法规技术服务商。我司可以办理:1:欧盟MDR CE咨询,MDR欧盟授权代表,欧盟注册2:欧盟IVDR CE咨询,IVDR欧盟授权代表,欧盟注册3:美国FDA注册,FDA510K4:国内的注册证和生产证5:加拿大的MDEL注册6:ISO13485咨询和认证目前SUNGO在中国、欧洲、北美和澳洲均设有服务机构,服务过..
- 我要给“FDA验厂的资料和费用 欢迎在线咨询”留言
- 更多产品
相关分类